AP.
Se avecinan cambios en el pasillo de medicamentos para la tos y el resfriado de su farmacia local: las autoridades estadounidenses están tomando medidas para eliminar gradualmente el principal descongestionante que se encuentra en cientos de medicamentos de venta libre, concluyendo que en realidad no alivia la congestión nasal.
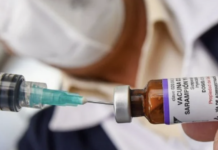
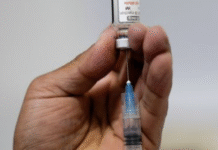
La fenilefrina se utiliza en versiones populares de Sudafed, Dayquil y otros medicamentos, pero los expertos han cuestionado su eficacia durante mucho tiempo. El mes pasado, la Administración de Alimentos y Medicamentos propuso formalmente revocar su uso en pastillas y soluciones líquidas, lo que dio inicio a un proceso que probablemente obligará a los fabricantes de medicamentos a retirar o reformular productos.
Es una victoria para los académicos escépticos, incluidos los investigadores de la Universidad de Florida que solicitaron a la FDA que revisara el uso del medicamento en 2007 y nuevamente en 2015. Para los consumidores, probablemente significará cambiar a alternativas, incluido un descongestionante más antiguo que se trasladó detrás del mostrador de la farmacia hace casi 20 años.
Los médicos dicen que los estadounidenses estarán mejor sin fenilefrina, que a menudo se combina con otros medicamentos para tratar el resfriado, la gripe, la fiebre y las alergias.
“Hoy en día, la gente entra en una farmacia y ve 55.000 medicamentos en los estantes, y elige uno que definitivamente no va a funcionar”, dijo el Dr. Brian Schroer de la Clínica Cleveland. “Si eliminamos esa opción, será más fácil para ellos elegir por sí mismos los productos que realmente los ayudarán”.
¿Por qué la FDA hace esto ahora?
La decisión de la FDA se esperaba después de que el año pasado los asesores federales votaran por unanimidad que no se ha demostrado que los medicamentos orales con fenilefrina alivien la congestión.
Los expertos analizaron varios estudios recientes de gran envergadura que indicaban que la fenilefrina no era mejor que un placebo para despejar las fosas nasales. También revisaron estudios de los años 1960 y 1970 que respaldaban el uso inicial del fármaco y encontraron numerosos fallos y datos cuestionables.
La opinión del panel sólo se aplica a la fenilefrina en medicamentos orales, que representan aproximadamente 1.800 millones de dólares en ventas anuales en Estados Unidos. El fármaco todavía se considera eficaz en aerosoles nasales, aunque estos son mucho menos populares.
La fenilefrina no siempre fue la mejor opción para los productos contra el resfriado y las alergias. Muchos de ellos se formulaban originalmente con un fármaco diferente, la pseudoefedrina.
Pero una ley de 2006 exigió a las farmacias que vendieran los productos con pseudoefedrina en mostradores, alegando su potencial para ser procesados en metanfetamina. Empresas como Johnson & Johnson y Bayer decidieron reformular sus productos para mantenerlos fácilmente disponibles en los estantes de las tiendas, y etiquetaron muchos de ellos como versiones “PE” de marcas conocidas.
¿Cuáles son algunas alternativas para la congestión?
Los consumidores que aún quieran tomar pastillas o jarabes para aliviar el dolor probablemente tendrán que acudir al mostrador de la farmacia, donde las versiones de Sudafed, Claritin D y otros productos que contienen pseudoefedrina siguen estando disponibles sin receta médica. Los compradores deben presentar un documento de identidad con fotografía.
Más allá de esos productos, la mayoría de las otras opciones son aerosoles o soluciones nasales de venta libre.
Las gotas y enjuagues salinos son una forma rápida de eliminar la mucosidad de la nariz. Para aliviar a largo plazo la congestión nasal, la picazón y los estornudos estacionales, muchos médicos recomiendan esteroides nasales, que se venden como Flonase, Nasacort y Rhinocort.
“Estos medicamentos son, con diferencia, el tratamiento diario más eficaz para la congestión y la congestión nasal”, afirmó Schroer. “El mayor problema es que no son muy eficaces cuando se utilizan según las necesidades”.
Los esteroides nasales generalmente deben usarse a diario para que sean altamente efectivos. Para un alivio a corto plazo, los pacientes pueden probar aerosoles antihistamínicos, como Astepro, que actúan más rápido.
Los aerosoles a base de fenilefrina también permanecerán en los estantes de las farmacias.
¿Por qué la fenilefrina no funciona cuando se toma por vía oral?
Los expertos que cuestionaron la eficacia del medicamento dicen que éste se descompone rápidamente y se vuelve ineficaz cuando llega al estómago.
“Es un buen fármaco, pero no cuando se ingiere”, dijo Leslie Hendeles, profesor emérito de la Facultad de Farmacia de la Universidad de Florida, donde fue coautor de varios artículos sobre el ingrediente. “Se inactiva en el intestino y no llega al torrente sanguíneo, por lo que no puede llegar a la nariz”.
Cuando Hendeles y sus colegas presentaron por primera vez una petición a la FDA sobre la fenilefrina, sugirieron que una dosis más alta podría ser eficaz. Pero estudios posteriores demostraron que incluso dosis un 400% superiores a las recomendadas actualmente no sirven para tratar la congestión nasal.
La FDA y otros investigadores concluyeron que aumentar aún más la dosis podría conllevar riesgos de seguridad.
“Si se usan dosis muy altas, el riesgo es que la presión arterial aumente tanto que podría ser peligroso para los pacientes”, dijo Randy Hatton, profesor de la Universidad de Florida que codirigió la investigación sobre la fenilefrina.
Debido a sus efectos cardiovasculares, el medicamento se utiliza a veces para tratar la presión arterial peligrosamente baja durante una cirugía, señaló Hatton.
¿Qué pasa después?
Los medicamentos orales a base de fenilefrina seguirán estando entre nosotros por un tiempo.
Los reguladores gubernamentales deben seguir un proceso público de varios pasos para eliminar el ingrediente de la lista de la FDA de medicamentos aprobados para descongestionantes de venta libre.
Durante seis meses, la FDA debe recibir comentarios sobre su propuesta, incluidos los de los consumidores y las empresas. Luego, la FDA debe analizar los comentarios antes de emitir una orden final. Incluso después de que se haya tomado esa decisión, es probable que las empresas tengan un año o más para retirar o reformular los productos.
Los fabricantes de medicamentos podrían retrasar aún más el proceso solicitando audiencias adicionales a la FDA.
Por ahora, la Asociación de Productos Sanitarios para el Consumidor (Consumer Healthcare Products Association), que representa a los fabricantes de medicamentos, quiere que los productos sigan disponibles y afirma que los estadounidenses merecen “la opción de elegir los productos que prefieren para el cuidado personal”.
Hatton dice que él y sus colegas no están de acuerdo: “Nuestra posición es que elegir algo que no funciona no es realmente una elección”.
___
El Departamento de Salud y Ciencia de Associated Press recibe apoyo del Grupo de Medios Educativos y Científicos del Instituto Médico Howard Hughes. AP es la única responsable de todo el contenido.